天津市索维电子技术有限公司 天津市 300000
摘要:光学相干层析成像(Optical Coherence Tomography,OCT)是一种基于光的低相干干涉原理的光学成像技术,以无损、非接触、速度快及精度高为主要特点。光学相干层析成像血流造影技术(Optical Coherence Tomography Angiography, OCTA)是一种基于OCT的新型无创血流影像检测技术,无需荧光标记或其他外源造影对比剂,便可获得眼底毛细血管形态、灌注以及血流动力学信息。
关键词:光学相干层析 OCTA 视网膜 血流造影
1 引言
光学相干层析(Optical Coherence Tomography,OCT)是一种光学断层扫描成像技术。OCT利用光在组织中的穿透特性和散射特性,返回的光信号携带了组织中不同深度的特征信息,经过光电转换,重构成为该组织的断层图像,可以为疾病的早期诊断提供直观的判断依据,提高微观诊疗水平。无损、非接触、速度快及精度高等特点使得以OCT为代表的微观影像成为当前医院影像学发展的主要趋势之一。
OCT技术首次应用于医学是在20世纪90年代初,作为一种光学测距技术(optical coherence-domain relfectometry,OCDR)的延伸[1],在眼睛等透明组织成像中,OCT的探测深度可以达到2cm以上[2][3] ,在皮肤等高散射组织中,也可以达到皮下1-2mm[4]。OCT作为一种医学成像技术,主要性能为成像深度,成像分辨率及成像速度等方面,而这些与宽带光源的性能和光电转换元件息息相关。1991年,美国MIT的D. Huang等人最先提出光学相干层析的概念,由此拉开了OCT技术飞速发展的序幕[5]。光相干断层扫描血管成像(Optical Coherence Tomography Angiography, OCTA)是一种基于OCT的新型无创血流影像检测技术,无需荧光标记或其他外源造影对比剂,便可获得眼底毛细血管形态、灌注以及血流动力学信息,目前开始逐步应用于眼科疾病的研究中,应用前景非常广阔。
2 OCT和OCTA原理
OCT是一种基于光的干涉的技术,以宽带光源的低相干干涉为基本原理,其系统结构如图1所示。

图1 OCT系统结构
迈克尔逊干涉仪是OCT的基本架构,宽带光源发出低相干光,经干涉系统分成两束,即参考光和样品光。参考光进入参考臂经反射镜反射回到干涉仪,样品光照射到所测量的组织上,产生的后向散射光返回进入干涉仪,两束返回光发生干涉并由光谱仪进行光电转换。由于宽带光源的相干距离非常短,一般在微米量级,只有在相干窗口内的两束返回光才可以发生干涉,即OCT的分辨率在微米量级。
由OCT硬件系统对眼底组织原始光谱信号的采集。OCT系统采用低相干光源,光学扫描系统会进行特殊编程来配合系统进行图像采集。图2描述了OCT光学扫描系统在进行血流造影模式下的特殊扫描模式,即同一横向位置进行重复性扫描的三维扫描模式,根据设计的簇内B-scan个数来调整扫描系统驱动信号锯齿波相对阶梯波的周期。最后由光谱仪完成对原始数据的获取工作。
对光谱仪采集到的原始光谱数据,进行波数校正和傅里叶变换的预处理,可以被解析成用振幅信息和相位信息表示的复数信号Ã(z,x):
![]()
 其中 Ã(z,x)表示经过波数校正傅里叶变换后得到的复数信号,z表示深度方向坐标,x表示沿振镜快速扫描方向坐标,Ioct(k,x)表示波数校准后的OCT光谱信号,k表示波数坐标,I(z,x)表示振幅图像信号,i表示虚数单位,φ(z,x)表示相位图像信号。
其中 Ã(z,x)表示经过波数校正傅里叶变换后得到的复数信号,z表示深度方向坐标,x表示沿振镜快速扫描方向坐标,Ioct(k,x)表示波数校准后的OCT光谱信号,k表示波数坐标,I(z,x)表示振幅图像信号,i表示虚数单位,φ(z,x)表示相位图像信号。

图2 OCTA扫描模式
在OCT数据采集过程中,眼底的同一位置处重复扫描采集到的B-scan图像为一组B-scan簇。由于呼吸心跳等自主运动会引发运动伪影,运动伪影会使同一位置的图像发生错位,使得数据失去连续性,难以分清静态和动态组织。在进行血流图像计算前,预先对簇内B-scan进行图像配准。采用基于振幅信息的配准算法,通过计算相邻图像的最大互相关值,获得深度和轴向的位移值,实现对B-scan相邻图像的配准。
生物组织静态部分在OCT图像里拥有相对稳定的振幅和相位值,当某处出现流动的血流时,图像对应位置的振幅和相位信息会发生波动,因此,振幅和相位的波动通常用来提取血流信息。当血流运动较小时,振幅变化幅度较小,仅相位会发生较大变化,相位的变化同样会反应到复信号图像上,OCT复信号对血流变化更加敏感。对相邻复信号图像进行差值运算,可以有效降低静态组织位置的复信号的实部和虚部数值,因为血流位置的复信号本身的幅间波动,差值运算并不会对血流位置的复信号产生和静态组织信号相同的效果。对经过差值运算的图像进行图像强度均衡归一化处理,即可得到最终的血流造影图像。
3 OCTA实验及结果
为了模拟人体组织中血流的实际情况,选择直径1mm的玻璃毛细管作为血管模型,选择牛奶作为血液模型,使用小型循环装置将牛奶匀速注入玻璃毛细管,用以模拟血液在管中流动的状态。同时,使用OCT设备对正在流动牛奶的玻璃毛细管进行特殊模式的采样,其中所采集的OCT图像如图3所示:
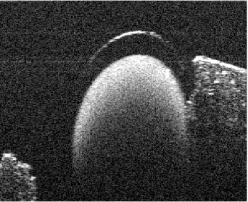
图3 仿真模型图像
将所采集的一组图像进行计算,玻璃毛细管及周边固定部分的信号被分离,只有通过流动牛奶位置的信号被保留下来,证明研究的光学相干层析成像血流造影技术可以实现。
为进一步验证研究技术的实用性,使用OCT设备对人眼黄斑区域进行信号采集,采集区域约为3mm×3mm,得到的黄斑区域血流造影图像如图4所示。


图4 人眼活体黄斑区血流造影图像
4 总结
OCT作为近年来飞速发展的光学技术,已经越来越多的被人们关注,并且在一些领域已经形成比较成熟的方案,为医学的进步发展提供了帮助。OCTA也凭其独特的优势在眼科等众多医疗领域崭露头角。随着OCT和OCTA技术的成熟与发展,OCT和OCTA在医学基础研究和临床应用方面都存在着巨大的发展潜力和广阔的发展前景。
参考文献
[1]R. C. Youngquist, S. Carr, and D. E. N. Davies, “Optical coherence domain reflectometry: A new optical evaluation technique,” Opt. Lett.,vol. 12, pp. 158–160, 1987.
[2]M. R. Hee, J. A. Izatt, E. A. Swanson, D. Huang, C. P. Lin, J.S. Schuman, C. A. Puliafito, and J. G. Fujimoto, “Optical coherencetomography of the human retina,” Arch. Ophthalmol., vol. 113, pp.326–332, 1995.
[3]S. A. Boppart, M. E. Brezinsk, B. E. Boump, G. J. Tearney, and J.G. Fujimoto, “Investigation of developing embryonic morphology usingoptical coherence tomography,” Dev. Biol., vol. 177, pp. 54–64, 1996.
[4]J. A. Izatt, M. D. Kulkarni, H. W.Wang, K. Kobayashi, and M. V. Sivak,“Optical coherence tomography and microscopy in gastrointestinal tissues,”IEEE J. Select. Topics Quantum Electron., vol. 2, pp. 1017–1028,1996.
[5]HUANGD,SWANSON E A,LIN C P,et al. Optical coherence tomography [J]. Science,1991,254 ( 5035 ) : 1178 -1181.