天津市南开中学滨海生态城学校 天津 300110
摘要:人教版高中化学19版新教材与旧教材在“关于外界条件对反应速率的影响”一节的设置有很大区别,本文从课本内容安排、实验的可行性、实验效果、学情等角度进行研究分析,以学生初中所学铁与稀硫酸的反应为载体,从温度、浓度、接触面积、原电池4个角度探究外界条件对反应速率的影响,丰富学生的视野,启发学生的思维。
关键词:人教版;反应速率;研究分析
一、问题由来
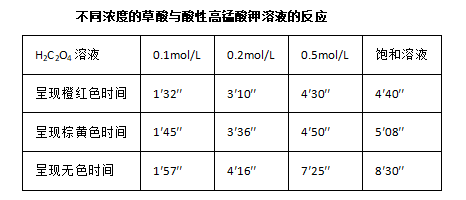
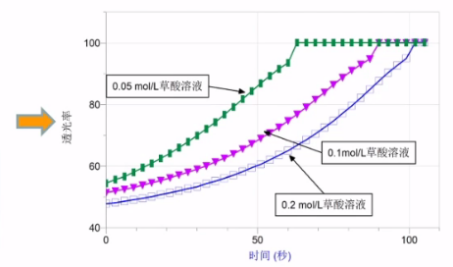
化学反应速率在高中化学教学中占有非常重要的地位,对学生理解化学反应的本质具有重要意义。人教版旧教材中研究影响反应速率的因素在选修四中有详尽的说明,以三个不同的反应从温度、浓度、催化剂三个角度对这一原理进行了探究:以草酸与酸性高锰酸钾溶液的反应为载体探究浓度对反应速率的影响;以硫代硫酸钠与硫酸的反应为载体探究温度对反应速率的影响;以双氧水的分解实验为载体探究催化剂对反应速率的影响,每一个反应对应一个探究的外界条件。而实验2-2中草酸与酸性高锰酸钾的实验不容易成功,多次试验的结果都是0.1mol/L的草酸先于0.2mol/L的草酸使酸性高锰酸钾溶液褪色,颜色由紫色-橙红色-棕黄色-无色,并不是颜色逐渐变浅直至无色,且颜色褪色速度先缓慢后加快。这是由于反应并非一步完成。在酸性较大的高锰酸钾溶液中加入草酸,当草酸浓度较小时以高锰酸钾的自身分解为主,而当草酸浓度较大时,反应过程步骤繁多,有些步骤反应较慢,所以褪色较慢,出现了与预期相反的结论。经实验验证,该反应褪色的时间还与溶液的酸性强弱有关。而19版新教材必修二实验活动7以“硫代硫酸钠与硫酸的反应”为载体,探究了温度、浓度两个因素对化学反应速率的影响。很显然,以一个反应为载体,可排除专一性,更有助于学生理解不同条件对反应速率的影响。“硫代硫酸钠与硫酸的反应”实验现象明显,快慢适中,但两组实验均为试管实验,产生有毒的二氧化硫气体,不符合绿色环保的理念,且探究的外界条件只有温度和浓度。根据学生已有的知识与经验,能否找到一个绿色环保的反应体系从更多的角度探究外界条件对反应速率的影响呢?本文以学生熟悉的初中所学的铁与稀硫酸的反应为载体,从温度、浓度、接触面积、原电池四个角度进行探究。
草酸滴入酸性高锰酸钾溶液的反应历程:
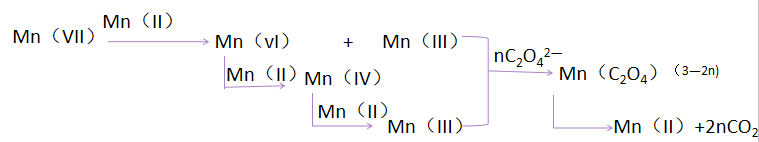
实验探究
【探究一】:浓度对反应速率的影响:取两只大小相同的试管,分别加入0.1mol/L和1mol/L硫酸溶液5mL,向两只一样的气球中分别加入2g铁粉,分别套在两支试管口,同时将气球中铁粉加入到试管中,通过观察试管中反应的剧烈程度、气球鼓起的先后以及试管的温度三个方面比较反应速率的大小。
【现象】现象:加1mol/L硫酸溶液的试管上方气球先鼓起,反应更剧烈,触摸试管壁温度更高。
【结论】:增大浓度,加快反应速率。
【探究二】:温度对反应速率的影响:取两只大小相同试管,分别加入1mol/L硫酸溶液各5mL,将两支分别置于盛有冰水和沸水的两个烧杯中,向两只一样的气球中分别加入2g铁粉,分别套在两支试管口,5分钟后同时将气球中铁粉加入到试管中,通过观察试管中反应的剧烈程度、气球鼓起的先后比较反应速率的大小。
【现象】现象:置于沸水中试管上方的气球先鼓起,反应更剧烈。
【结论】:升高温度,加快反应速率。
【探究三】:接触面积对反应速率的影响:取两只大小相同试管,分别加入1mol/L硫酸溶液各5mL,向两只一样的气球中分别加入2g铁粉,分别套在两支试管口,同时将气球中铁粉加入到试管中,向其中一支试管的底部放一块磁铁,通过观察试管中反应的剧烈程度、气球鼓起的先后以及试管的温度比较反应速率的大小。
【现象】现象:未放磁铁的试管上方的气球先鼓起,反应更剧烈,温度更高。
【结论】:减小接触面积,减慢反应速率。反之,增大接触面积,加快反应速率。
【探究四】:原电池对反应速率的影响:向装有5mL1mol/L的硫酸溶液的两只试管中分别加入1mL1mol/L硫酸铜溶液和1mL蒸馏水,后同时加入2g铁粉。通过观察试管中反应的剧烈程度、气球鼓起的先后以及试管的温度比较反应速率的大小。
【现象】滴入蒸馏水的试管上方气球先鼓起
 【思考】:可能原因:Fe+2H+=Fe2++H2 滴加蒸馏水的试管中直接发生产生氢气的反应,由于铜离子的氧化性强于氢离子,滴加硫酸铜溶液的试管中铁先与铜离子反应,后发生铁与氢离子的反应。由于氢离子浓度过高,反应速率过快,滴加蒸馏水的试管上方气球先鼓起。
【思考】:可能原因:Fe+2H+=Fe2++H2 滴加蒸馏水的试管中直接发生产生氢气的反应,由于铜离子的氧化性强于氢离子,滴加硫酸铜溶液的试管中铁先与铜离子反应,后发生铁与氢离子的反应。由于氢离子浓度过高,反应速率过快,滴加蒸馏水的试管上方气球先鼓起。
【改进1】向装有5mL0.1mol/L的硫酸溶液的两只试管中分别加入1mL1mol/L硫酸铜溶液和1mL蒸馏水,后同时加入2g铁粉。通过观察试管中反应的剧烈程度、气球鼓起的先后比较反应速率的大小。
【现象】滴入蒸馏水试管上方气球先鼓起。滴入硫酸铜溶液的试管红产生大量红色固体。
【思考】:接触面积影响固体反应速率,是否因为产生的铜过多覆盖在铁表。面影响了反应速率呢?
【改进2】向装有5mL0.1mol/L的硫酸溶液的两只试管中分别加入2滴1mol/L硫酸铜溶液和2滴蒸馏水,后同时加入2g铁粉。通过观察试管中反应的剧烈程度、气球鼓起的先后以及试管的温度比较反应速率的大小。
【现象】滴硫酸铜溶液的试管中溶液更浑浊,反应更剧烈。气球鼓起不明显。
【改进3】向装有5mL2mol/L的硫酸溶液的两只试管中分别加入2滴硫酸铜溶液和2滴蒸馏水,后同时加入2g铁粉。通过观察试管中反应的剧烈程度、气球鼓起的先后以及试管的温度比较反应速率的大小。
【现象】滴硫酸铜溶液的试管上方的气球先鼓起,试管中溶液更浑浊,反应更剧烈。
【结论】:形成原电池,能加快反应速率。
【思考与交流】向装有5mL1mol/L的硫酸溶液的两只试管中分别加入1mL1mol/L硫酸铜溶液和1mL蒸馏水,后同时加入2g铁粉,刚开始滴蒸馏水的试管上方气球先鼓起。放置1小时以后,滴入硫酸铜试管上方的气球反而更大,试管中反应更剧烈,这是为什么呢?
【结论】随着反应的进行,影响反应速率的因素不止一个。在不同时刻起决定作用的因素不同。
三、教学反思
化学反应速率的影响因素为19年人教版新教材必修课程学生必做实验之一,根据学生已有生活经验,不难设计出温度、浓度两外界因素对反应速率的影响,结合煤炭燃烧,可以引导学生设计出接触面积对反应速率的影响。以铁与稀硫酸的反应为例进行探究,用铁块和铁粉参与反应进行反应速率的比较,但可能由于来源不同,纯度不同造成干扰。本实验利用铁可以被磁铁吸引这一性质,采用逆向思维,向试管中同时加入等量的分析纯铁粉,立即向一支试管底部放一块磁铁,将铁粉迅速吸引到底部聚集在一起,另一只试管中的铁粉慢慢散落,接触面积较大,从接触面积的角度对反应速率进行比较。通过19版新教材必修二第六章第一节化学反应与能量的变化的学习,学生已有原电池的相关知识,可以引导学生设计原电池,探究原电池对反应速率的影响。在该组实验探究过程中,出现滴加蒸馏水的试管先鼓起的“异常现象”,借此机会引导学生反思,改进实验方案,在实践中总结经验,提出自己的看法,可以提高学生运用所学化学知识解决实际问题的能力,鼓励学生从多角度分析解决实际问题,培养学生的发散思维和创新精神。让学生亲身体验本次实验如果结合数字化实验如压强传感器、氢气传感器、温度传感器等效果更明显。
参考文献:
王春.草酸与高锰酸钾反应的原理探究与改进建议[J].化学教育,2010(5)
 江双青.一箭双雕 学生分组实验创新设计两例[J].化学教育学,2018(12)
江双青.一箭双雕 学生分组实验创新设计两例[J].化学教育学,2018(12)