袁雪芬
乌鲁木齐市第十二中学 新疆 乌鲁木齐830000
【摘要】自发的氧化还原反应形成原电池,氧化剂与还原剂不接触也是可以反应的,就要根据组成电池的电动势差来判断。化学学科核心素养,其中宏观辨析与微观探析、变化观念与平衡思想,这两方面阐明了:能从不同层次认识物质的多样性;能认识物质是运动和变化的,知道化学变化需要一定的条件,并遵循一定规律;认识化学变化有一定限度,是可以调的。
关键词:原电池;氧化还原反应;电势差
核心素养是党的教育方针的具体化,是连接宏观教育理念,培养目标与具体教育教学实践的中间环节。党的教育方针通过核心素养这一桥梁,可以转化为教育教学实践可用的,教育工作者易于理解的具体要求。明确学生应具备的必备品格和关键能力,从中观层面深入回答“立什么德、树什么人”的根本问题,引领课程改革和育人模式变革。化学学科核心素养,其中宏观辨析与微观探析、变化观念与平衡思想,这两方面阐明了:能从不同层次认识物质的多样性;能认识物质是运动和变化的,知道化学变化需要一定的条件,并遵循一定规律;认识化学变化有一定限度,是可以调的。
在讲解人教版选修四《原电池 原理》时,关于原电池形成条件之一:自发的氧化还原反应。何为“自发”,就是学生认识化学变化虽有一定限度 ,但是可以调的。
原电池是可以将化学能转化为电能的装置。形成原电池条件是1、自发的氧化还原反应;2、电解质;3、导电的两极(一般活泼性有差异);4、闭合回路。形成电流的首要条件是:自发的氧化还原反应要分两处进行。即,负极发生氧化反应,正极发生还原反应。这样电子定向移动从而形成电流。因此,装置图探究过程如下:
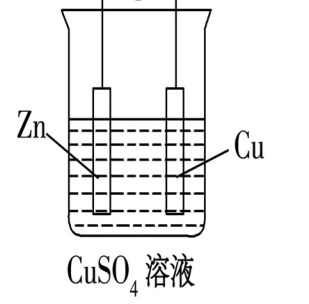
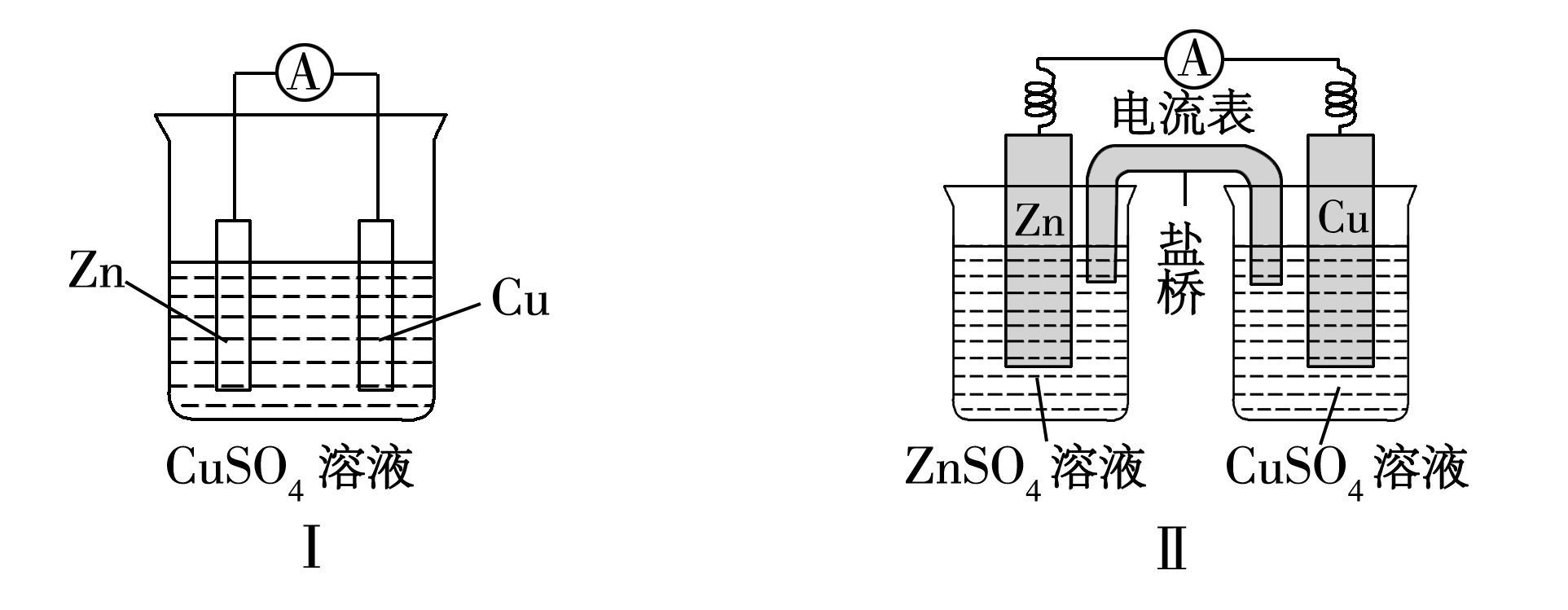
图1 图2
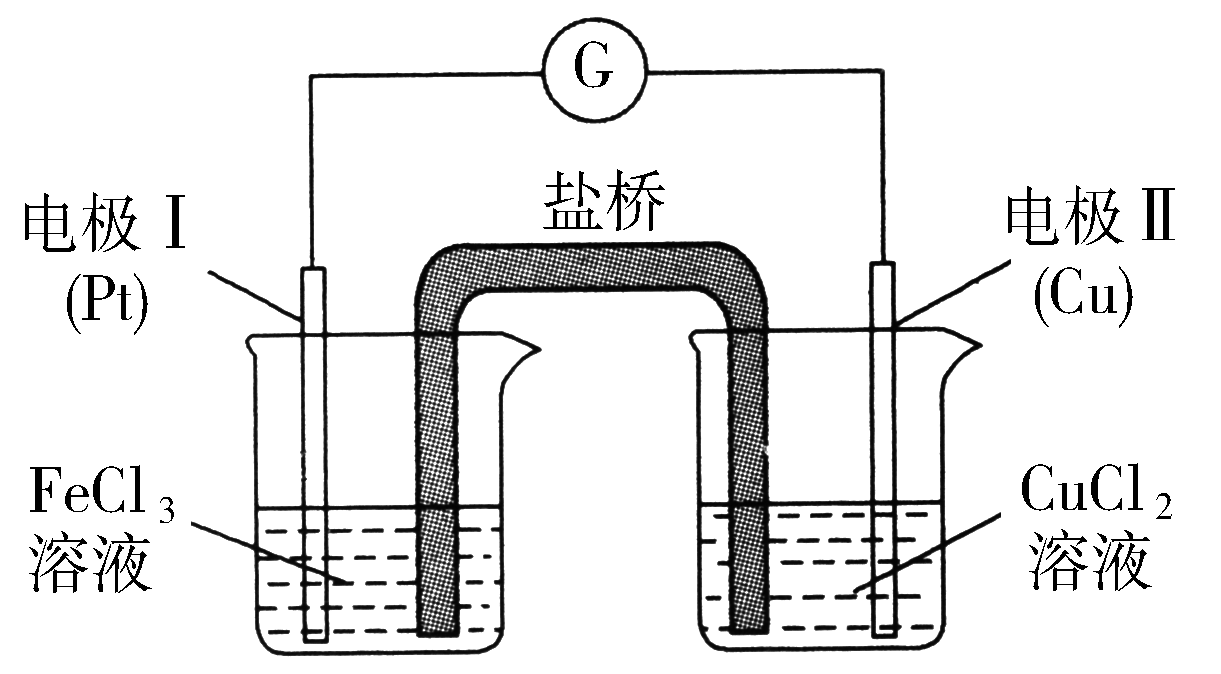
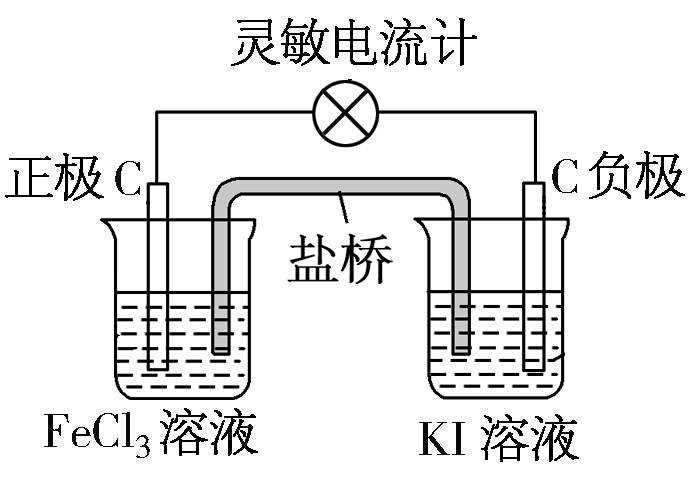
图3 图4
图1没有形成闭合回路,锌与硫酸铜反应在锌棒发生,电子不能发生定向移动,形成不了电流,因此该装置不能构成原电池。图2Ⅰ构成原电池,锌作负极:Zn-2eˉ=Zn2+ ;铜作正极:Cu2++2eˉ=Cu。氧化剂与还原剂直接接触发生反应。这也是给学生在学习过程中造成错误的理解。即,氧化剂与还原剂直接接触才可以发生反应,或者只要是氧化剂,还原剂就能发生反应。所以设计了图2Ⅱ,锌与硫酸铜溶液没有接触,通过搭盐桥形成闭合回路,发生原电池反应。改变了学生对原电池反应的看法,氧化剂与还原剂不接触也是可以发生反应的。这是因为金属单质本身就会失电子,存在自由移动的电子。只要可以形成闭合回路,电子顺着导线来到正极,氧化性强的微粒就会在正极得电子,产生电流。如图3,自发的总反应:Cu+2Fe3+=2Fe2++Cu2+,所以,电极Ⅱ为负极:Cu—2eˉ= Cu2+ ;电极Ⅰ为正极:2Fe3++ 2eˉ=2Fe2+。
那么图4,学生理解的就很难了。电极材料都是碳棒,决定这个装置是否能构成原电池,取决于2Fe3++2Iˉ=2Fe2++I2反应是否自发?然而,原电池发生的氧化还原反应是否自发如何判断呢?在中学的教材学习中是受限的,只有去查阅资料,解决这个问题。
利用氧化还原反应所组成的电池的电动势(指电池正、负极之间的平衡电势差)来判断。当电池中两个电极之间电势差大于+(0.2-0.4)或小于-(0.2—0.4)时,可直接作为反应自发性的判据。否则要考虑浓度的影响,高温熔融盐的电极反应不能用这些数据使用。查阅电极电势表格得到数据:Eθ I2/Iˉ=+0.54V; EθFe3+/Fe2+=+0.77V;两极电势差为+0.23V,大于+(0.2-0.4),该反应自发。形成原电池,是有电流产生的。负极:2Iˉ-2eˉ=I2;正极:2Fe3++ 2eˉ=2Fe2+。
这就打破了,学生的认知,即:自发的氧化还原反应形成原电池,氧化剂与还原剂不接触也是可以反应的。因此,发生于原电池反应的首要条件是有自发的氧化还原反应,而判断反应的自发性要根据电池两个电极之间的电势差判据。
高中化学教学的目标不仅仅是应试,更重要的是让学生具备较完备的学科知识体系和学习能力,并为此基础上培养学生的学科素养。所以,在平时的教学中,教师有意识的培养学生的化学学科素养,特别是核心素养,将极大的提升学生在化学学科的学习能力,教学中只有着眼于学生长远能力的提升,用“上台阶”式的教学设计有条不紊的进行培养,学生的学科素养方能得到加强,为中国新时代社会主义培养新时代社会主义接班人,实现伟大的中国梦。
【参考文献】
1、《基于学科核心素养的化学教学课例研究》刘翠 华东师范出版社
2、《无机化学》高等教育 人民教育出版社
3、《高中化学学科核心素养解读》 匆雨来了微博 2017年8月